A1 、主な構成部品
正極板 二酸化鉛( PbO2 )
負極板 鉛( Pb )
電解液 希硫酸 ( 濃度 30 〜 35 %)『硫酸( H2SO4 )+水( H2O )』
A2 、原理
電気エネルギーを 発生 ( 放電) させ、また逆に電気エネルギーを 蓄電 ( 充電) させる。
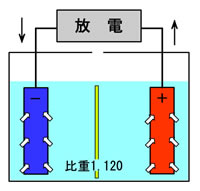
| 放電 |
バッテリーを放電すると硫酸分が極板に着く
陽極板は二酸化鉛 ( PbO2 ) → 硫酸鉛( PbSO4 ) へと変化する。
PbO2 → PbSO4
陰極板は海綿状鉛( Pb ) → 硫酸鉛( PbSO4 ) へと変化する。
Pb → PbSO4
希硫酸 『硫酸( H2SO4 )+水( H2O )』 は水( H2O )へと変化する為、
『硫酸( H2SO4 )+水( H2O )』の比率である 比重が低下する。
比重 1.120 |
 |
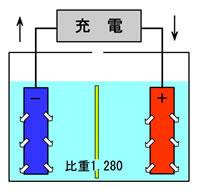
| 充電 |
陽極板は硫酸鉛( PbSO4 ) → 二酸化鉛 ( PbO2 ) へと変化する。
PbSO4 → PbO2
陰極板は硫酸鉛( PbSO4 ) → 海綿状鉛( Pb ) へと変化する。
PbSO4 → Pb
希硫酸 『硫酸( H2SO4 )+水( H2O )』 は 硫酸( H2SO4 ) へと変化する為、
『硫酸( H2SO4 )+水( H2O )』の比率である 比重が上昇する。
上記の化学反応により、イオン(電子)が生成され、銅線などに電気が流れる。
比重 1.280 |
 |
A3 、バッテリーの電圧
上記の原理で発電を行うと約 2.0V ほどの電気が発生する。自動車のバッテリーはこれを 6 個バッテリー内部で直結にしてある
2.0V × 6 個で 12V の電圧が発生しております。
A4, 放置期間と自己放電量
バッテリーは保管中でも自己放電により少しずつ放電します。
自己放電で失われた容量を回復させるためにも補充電が必要になります。
※ バッテリーは生きものです。充電、放電を繰り返さないと劣化致します。
放置後の再充電目安 夏期: 3 ヶ月に一度 冬期: 6 ヶ月に一度 |

